点击蓝字,关注我们

scDrugPrio:
分析单细胞转录组学的框架, 以解决免疫介导的炎症性疾病精准医学中的多个问题
scDrugPrio: a framework for the analysis of single-cell transcriptomics to address multiple problems in precision medicine in immune-mediated inflammatory diseases
摘 要
药物治疗效果不佳是许多免疫介导炎症性疾病(IMIDs)患者面临的主要问题。其重要原因是缺乏基于对免疫介导炎症性疾病复杂多变的细胞和分子变化特征进行药物优先排序和再利用的系统解决方案。
在此背景下研究人员提出了一个计算框架--scDrugPrio,它可以根据单细胞 RNA 测序(scRNA-seq)数据构建炎症性疾病的网络模型。scDrugPrio 构建了详细的炎症性疾病网络模型,该模型整合了细胞类型特异性表达变化、细胞串联改变和药理学特性等信息,可用于数千种药物的选择和排序。对个体患者的应用表明,scDrugPrio 具有在细胞组、基因组和药物组范围内进行基于网络的个性化药物筛选的潜力。为此,研究人员将 scDrugPrio 制作成了一个易于使用的R软件包
https://github.com/SDTC-CPMed/scDrugPrio。

01
研究概述
scDrugPrio 使用 1) 一个个体;2) 患者和对照之间的一组比较的 scRNA-seq 衍生的差异表达基因 (DEG),首先通过考虑蛋白质-蛋白质相互作用网络中的邻近性来识别细胞类型特异性候选药物和生物药理学标准。为了对候选药物进行排名,scDrugPrio 计算了两种度量:细胞内中心性和细胞外中心性。
研究人员使用这两种措施来捕获两个重要的药物特性,即 1)针对细胞类型中与疾病相关的关键表达变化的熟练程度;2)目标细胞类型的相对重要性。然后将所有细胞类型的这些测量结果进行汇总,以提供最终的药物排名。
scDrugPrio 是利用抗原诱发关节炎的小鼠模型开发的,通过提高已批准药物的精确度或召回率,以及对已预测但未批准用于所研究疾病的药物进行广泛的体外、体内和硅学研究,验证了 scDrugPrio 的有效性。接下来,scDrugPrio 被应用于多发性硬化症、克罗恩病和银屑病关节炎,通过对相关药物和已批准药物进行优先排序,进一步支持了 scDrugPrio。然而,与关节炎小鼠模型相比,在相同诊断的患者中发现个体间细胞和基因表达差异较大。这种差异可以解释为什么一些患者对治疗没有反应。该解释得到了 scDrugPrio 应用于来自 11 名个体克罗恩病患者的 scRNA-seq 数据的支持。分析表明,不同患者之间的药物预测存在很大差异,例如,对抗肿瘤坏死因子治疗有反应的患者药物预测等级较高,而对该治疗无反应的患者药物预测等级较低。
02
研究方法
01
整体流程
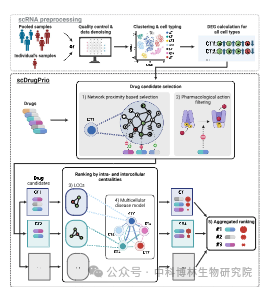
scDrugPrio工作流程概述样本来自患者的炎症组织(红色)和对照组的健康组织(蓝色),或者,对于个体预测,采样包括来自同一患者的炎症组织和未炎症组织。单细胞rna测序(scRNA-seq)对数据进行质控、去噪、聚类、细胞分型和差异表达基因(differential expression gene, DEG)计算等预处理。计算健康和患病样本之间每种细胞类型的DEGs。scDrugPrio使用DEGs和药物信息来选择候选药物(针对每种细胞类型;CT),其基因靶点(1)与DEGs网络接近(基于网络接近的选择),(2)抵消疾病相关的表达变化(药理作用过滤)。接下来使用细胞内和细胞间中心性对这些细胞类型特异性候选药物进行排名。(3)细胞内中心性是根据药物靶点在由DEGs组成的最大连接成分(LCC)中的中心性来计算的,并作为药物靶点重要性的代表。(4)细胞间中心性测量疾病相关细胞串扰网络的中心性,称为多细胞疾病模型(mcdm)。(5)为了得出将细胞类型特异性药物选择和排名汇总到一个列表中的最终排名,使用细胞内和细胞间中心性的综合评分对候选药物进行排名。具有相同靶点和作用机制的药物被给予相同的排名
02
scDrugPrio需要
(1)调整后的scRNA-seq矩阵;
(2)基于健康样本和患病样本的分组比较或来自一个个体的炎症样本和非炎症样本的每种细胞类型的疾病相关差异表达基因(DEGs);
(3)蛋白质-蛋白质相互作用网络(PPIN);
(4)药物靶点信息。
scDrugPrio利用这些信息进行细胞类型特异性药物选择、计算药物排名度量并最终进行排名汇总。除非另有说明,分析均在R 3.6.3中进行。此包与 R >= 3.6 兼容。依赖项:dplyr(>= 1.0.7)、Seurat(>= 3.1.0)、R.filesets(>= 2.12.1)、igraph(>= 1.2.6)、doParallel(>= 1.0.15)、CINNA(>= 1.1.51)、reshape2(>= 1.4.4)、ggplot2(>= 3.3.5)、nichesnetr(>= 1.0.0)、MAST(>= 1.19.0)、limma(>= 3.54.0)和 ComplexHeatmap(>= 2.14.0)。建议的软件包:RCurl、GEOquery、KEGGREST、KEGGgraph、devtools。
03
工作流程、输入和输出数据
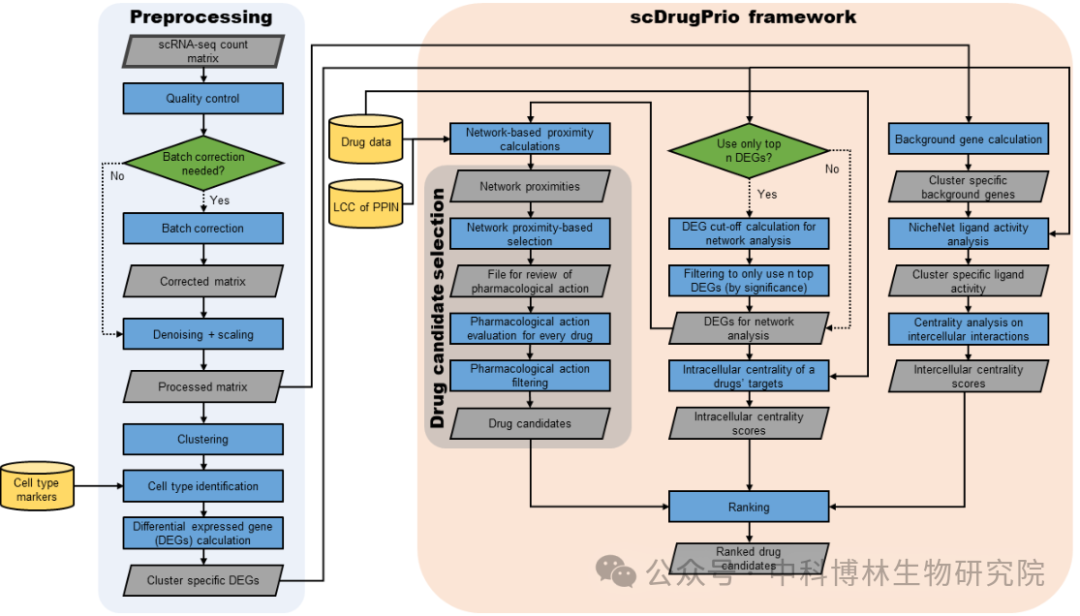
首先,按照标准方法对数据进行预处理,从而计算出患病细胞和健康细胞之间细胞类型特异性差异表达基因 (DEG)。通过异质性分析评估批次校正的必要性,如方法和补充方法部分所述。DEG 计算使用来自个体的配对样本(例如,一个健康样本和一个患病样本)或来自多个健康对照和患者的合并样本。然后,scDrugPrio 框架使用 DEG 和药物数据进行网络接近度计算,从而进行药物选择。使用细胞内和细胞间中心性将细胞类型特异性候选药物聚合成最终药物排名。灰色平行四边形表示数据文件,黄色圆柱体表示外部数据,绿色圆形表示决策点。
04
药物选择
药物选择针对每种细胞类型单独进行,包括网络接近度和药理作用过滤。首先,计算平均最近网络距离。有效候选药物的药物靶标与疾病相关 DEG 之间的平均网络距离往往小于预期,此外,它们往往至少直接针对疾病相关的 DEG。药理作用过滤遵循一个简单的假设,即药物需要抵消与疾病相关的表达变化才能治疗免疫介导的炎症疾病。为了检查这一点,我们将直接靶向 DEG 的倍数变化与对该靶标的预期药理作用进行了比较,并确定。
05
细胞间疾病模型
在选择药物后,scDrugPrio 将应用NicheNet 1来选择细胞类型之间的配体相互作用,这些相互作用可以预测下游细胞类型中观察到的转录组扰动。这允许创建一个有向多细胞疾病模型,该模型反映了疾病中细胞类型信号的改变。我们发现 MCDM 中的细胞类型中心性与细胞类型的 DEG 中 GWAS 富集的重要性以及疾病相关药物的预测精度密切相关。换句话说,针对 MCDM 中中心细胞类型的候选药物更有可能有效。
06
细胞内疾病模型
细胞内疾病模型是指对单个细胞类型中与疾病相关的变化进行建模。为此,我们使用基于网络的方法,将与疾病相关的 DEG 映射到 PPIN 上。使用 PPIN 中由细胞类型 DEG 形成的最大连通分量,我们可以确定每个 DEG 对细胞类型特定疾病的中心性。可以说,针对细胞类型中更中心的疾病相关转录组变化的药物将有更高的机会发挥作用。因此,scDrugPrio 计算了药物靶标在细胞类型特定疾病模块中的中心性。这被称为药物的细胞内中心性,并作为药物排名中药理学重要性的衡量标准。
07
药物排名
在选择药物并计算细胞间和细胞内中心性之后,对至少一种细胞类型的候选药物进行药物排名。对于每种药物,scDrugPrio 计算细胞间中心性的总和,仅包括该药物作为候选细胞类型。这可以作为药物所针对的细胞类型在 MCDM 中重要性的总体指标。接下来,scDrugPrio 计算药物候选物在所有细胞类型中的细胞内特征向量中心性的平均值,以得出指示药物对所有细胞类型的转录组变化的平均药理潜力的指标。最终排名基于细胞间中心性和细胞内中心性的综合得分。
03
参考文献
Schäfer S, Smelik M, Sysoev O, et al. scDrugPrio: A framework for the analysis of single-cell transcriptomics to address multiple problems in precision medicine in immune-mediated inflammatory diseases[J]. Genome Medicine, 2024, 16(1): 42.
—END—

中科博林

点
阅读原文 了解更多